蒸發(Evaporation)是指液體緩慢的由凝結態(液態)轉變為揮發態(氣態)的過程;凝結(Condensation)相對是指揮發態凝結形成液體的過程。這兩個過程會依據溫度變化而形成動態平衡,當溫度增加時,更多的物質會轉變為揮發態,反之亦然。
當分析樣品揮發時,其形成的揮發氣體將會推擠已存在的氣體形成蒸氣壓(vapor pressure);當溫度上升時,揮發的速率會上升並導致蒸氣壓的形成,溫度(以及蒸氣壓)可以持續上升直到與上述的液體壓力達到平衡,這個溫度即為物質的沸點,而此時物質將會由整個樣品開始揮發而不是僅僅只有表面開始。
不同的物質具有不同的蒸氣壓速率以及沸點溫度,正是這些差異使得不同的物質可以在氣相層析管柱中進行分離。
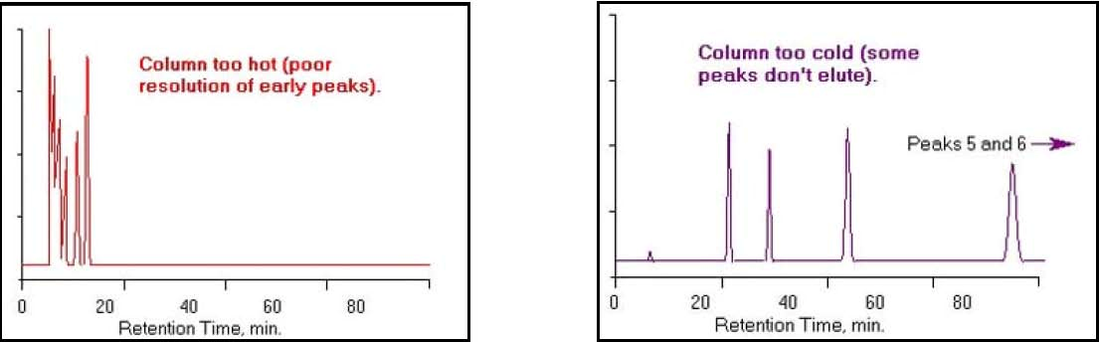
若烘箱溫度過低,分析物將會花更多的時間在穩定相中凝結,而只有少量的分析物可以揮發,由於液體轉變為氣體的過程太過於緩慢使得分析物的滯留時間過長;相對的,假設溫度太高,會使得氣液平衡偏向氣相,分析物在管柱中幾乎不會凝結進入穩定相(或是交互作用),會導致滯留時間太短。
氣相層析最好的運作環境是分析樣品可以在穩定相與氣相中達到動態平衡,理想的分離效果應該必須取得適當的溫度使得分析物可以穩定的進出穩定相,一般溫度設在分析物沸點下20-50℃之間。
等溫(isothermal)分離可以以這樣的溫度設定範圍來取得最佳的分離效果;若是要使用溫度程序梯度來取得問題分析物的最佳分離條件,建議梯度變化設定應當緩慢而不劇烈。
Key words: GC, temperature, retention time
Author: Kory Kelly
© 2009 Phenomenex, Inc. All rights reserved.
Web: www.Phenomenex.com Email: [email protected]
Author: Kory Kelly
© 2009 Phenomenex, Inc. All rights reserved.
Web: www.Phenomenex.com Email: [email protected]

 RSS Feed
RSS Feed